编译:高杰
每一天,
我们的大脑都在施展奇妙的魔法:
把稍纵即逝的印象、
一闪而过的灵感,
还有真切的情感体验,
转化成能长久留存的记忆。
而神经科学领域的一个
核心问题是——
大脑如何判定哪些信息值得储存?
以及
这些记忆应当保存多久?
最新研究发现,长期记忆的形成依赖于一系列分子计时机制,这些机制会在大脑不同区域依次激活。科学家借助针对小鼠的虚拟现实行为系统,发现了一些调控因子,它们要么助力记忆进入更稳定的状态,要么让记忆彻底消失。
11月26日,美国洛克菲勒大学发表在《自然》杂志上的这项研究强调,多个大脑区域会协同作用,随着时间的推移对记忆进行重组,其中的“检查点”会帮助评估每个记忆的重要性及其应有的持久性。
“这是一项关键发现,它解释了我们如何调整记忆的持久度,”神经动力学与认知实验室主任Priya Rajasethupathy表示,“我们选择记住什么,是一个持续演变的过程,而非一次性的开关切换。”

多年来,研究人员主要关注两个主要的记忆中枢:支撑短期记忆的海马体,以及被认为储存长期记忆的大脑皮层。此前观点认为,这些长期记忆的存储背后是受生物学开关的控制。
“大脑中现有的记忆模型涉及类似晶体管的记忆分子,它们扮演着开关的角色。” Rajasethupathy说。
这种传统观点认为,一旦某个记忆被标记为长期储存,就会永久存在。尽管这一框架提供了有用的见解,却无法解释为何有些长期记忆仅能维持数周,而有些却能清晰留存数十年。

2023年,Rajasethupath及其同事发现了一条连接短期与长期记忆系统的大脑回路。该通路的核心是丘脑,它负责筛选值得保留的记忆,并将其输送至大脑皮层进行长期稳定储存。
这些发现引出了更深层次的问题:记忆离开海马体后会发生什么?哪些分子过程决定了记忆是会持久留存还是消失殆尽?
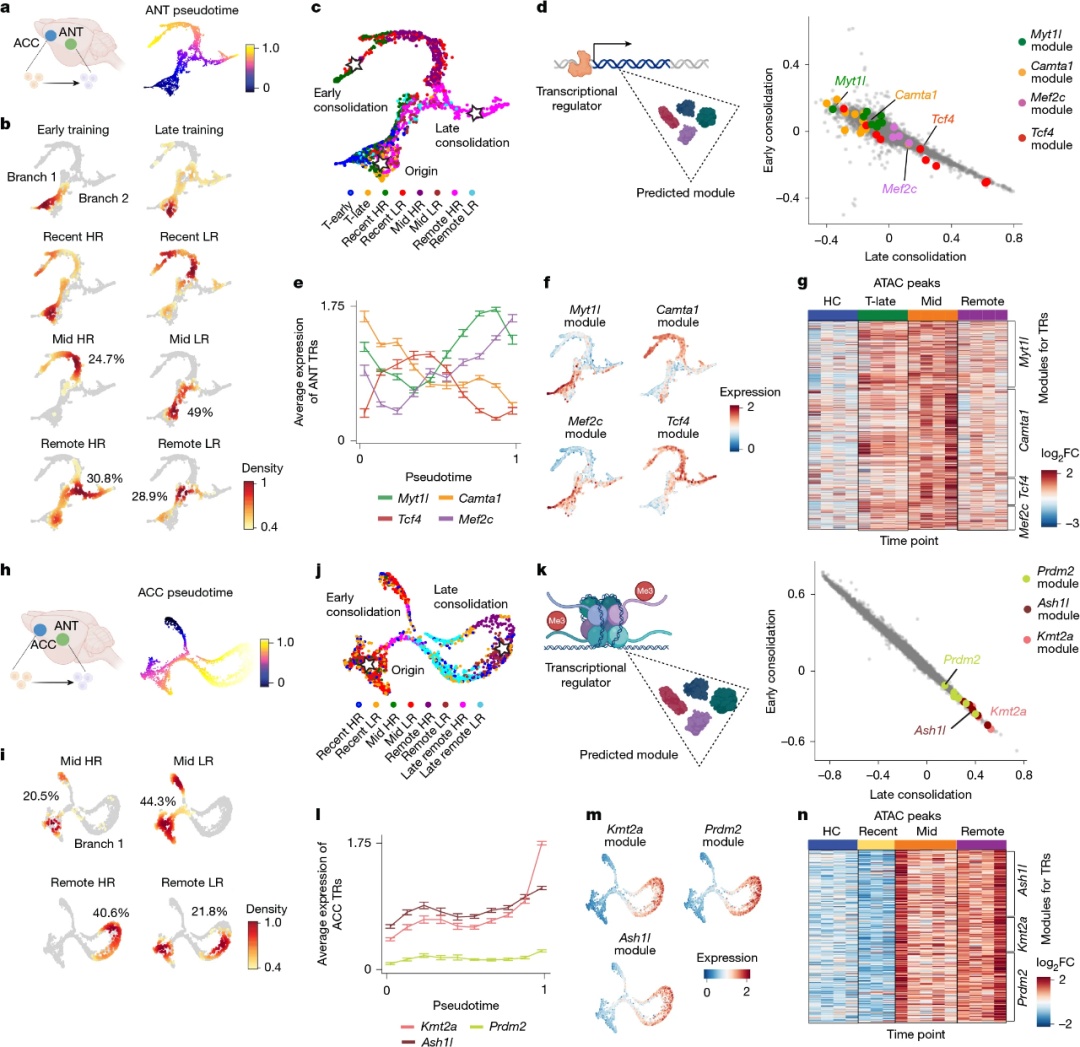
转录调控因子定义了与记忆持久性相关的表型状态进入
为探究这些机制,研究团队搭建了一套精妙的虚拟现实装置,让小鼠形成特定的记忆。“通过改变某些经历的重复频率,让小鼠对某些事物的记忆优于其他事物,随后深入观察大脑,找出与记忆持久性相关的机制。”
仅靠相关性无法解答核心问题,因此共同作者Celine Chen创建了基于CRISPR的筛选平台,用以改变丘脑和大脑皮层中的基因活性。这一方法显示,移除某些分子会改变记忆的持续时长,且每种分子都在其自身的时间尺度上运作。
研究结果表明,长期记忆的形成并非依赖单一的“开/关”开关,而是依靠一系列基因调控程序,这些程序如同分子计时器一样在大脑中逐步展开。
早期的计时器激活迅速但消退也快,会导致记忆消失;后期的计时器激活较慢,却能为重要经历提供持久所需的结构支撑。在该研究中,研究人员以“重复次数”作为衡量记忆重要性的指标,对比了频繁重复的场景与偶尔出现的场景对记忆的影响。

Camta1–Tcf4–Ash1l丘脑皮层转录级联反应是记忆稳定过程中必需的
团队发现了3种对维持记忆至关重要的转录调控因子:丘脑中的Camta1和Tcf4,以及前扣带回皮层中的Ash1l。这些分子并非形成初始记忆所必需,但对记忆的保存至关重要。干扰 Camta1和Tcf4会削弱丘脑与大脑皮层之间的连接,进而导致记忆丧失。
根据该模型,记忆形成始于海马体。Camta1及其下游靶标帮助维持早期记忆的完整性;随着时间推移,Tcf4及其靶标被激活,增强细胞黏附性和结构支撑;最终,Ash1l推动染色质重塑程序,进一步巩固记忆的稳定性。“
除非让记忆进入这些计时器的调控体系,否则它很快就会被遗忘。” Rajasethupathy说。
Ash1l属于组蛋白甲基转移酶蛋白家族,这类分子在其他系统中也参与维持类似记忆的功能。“在免疫系统中,这些分子帮助身体记住过往的感染;在发育过程中,它们又协助细胞记住自身已分化为神经元或肌肉细胞,并长期维持这一身份,”Rajasethupathy说,“大脑或许是借用了这种普遍存在的细胞记忆形式,来支撑认知层面的记忆。”
这些发现或许能最终帮助研究人员攻克与记忆相关的疾病。Rajasethupathy指出,通过理解保存记忆的基因程序,科学家有望在阿尔茨海默病等病症中,让记忆通路绕过受损的大脑区域。“如果我们知道记忆巩固的第二、第三个关键脑区,而第一个脑区的神经元正在死亡,或许就能绕过受损区域,让大脑的健康部分接管记忆功能。”
研究团队目前致力于揭示这些分子计时器的激活机制,以及是什么决定了它们的持续时间,包括探究大脑如何评估记忆的重要性并决定其保存时长。他们的研究继续指向丘脑是这一决策过程的核心枢纽。

数据图及参考来源:
https://www.nature.com/articles/s41586-025-09774-6
除已标注来源外,本文封面图及文内图片均来自包图网(获授权使用),转载可能引起版权纠纷。